Hipoxantina Além da xantina, é um produto de degradação do metabolismo das purinas. É posteriormente decomposto em ácido úrico. As doenças podem ocorrer quando sua degradação em ácido úrico é inibida e quando sua reciclagem pela via de recuperação é perturbada.
O que é hipoxantina?
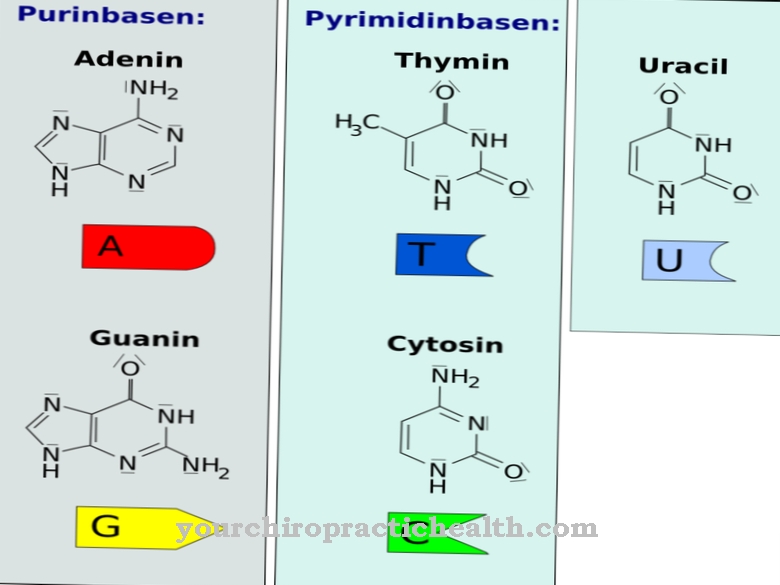
A hipoxantina é um derivado da purina e é produzida quando as bases da purina adenina e guanina são quebradas. Junto com a xantina, é um intermediário na síntese de ácido úrico. Sob a influência da xantina oxidase, a hipoxantina é geralmente primeiro decomposta em xantina e depois em ácido úrico.
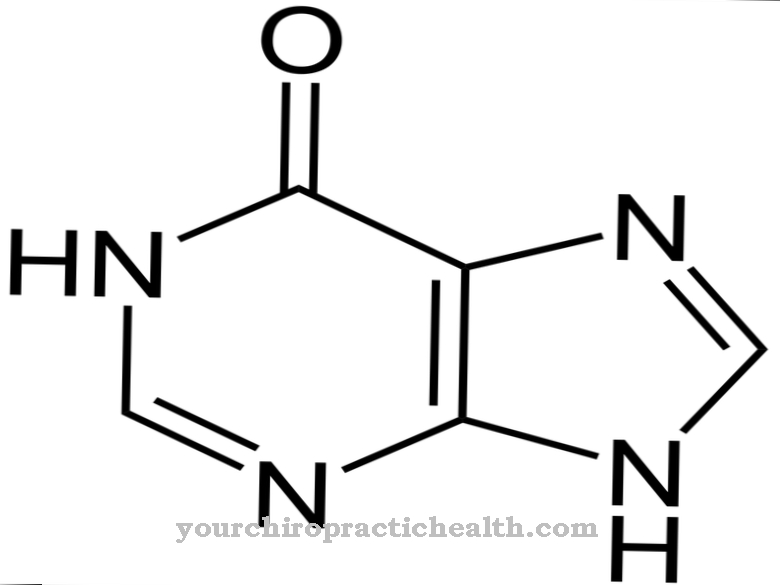
Como todos os derivados de purina, consiste em dois anéis heterocíclicos contendo seis ou cinco átomos. Há um total de nove átomos nos anéis. Existem cinco átomos de carbono e quatro de nitrogênio. Dois átomos de carbono pertencem a ambos os anéis. Um grupo hidroxila está ligado ao átomo de carbono na posição 6. Por meio dos efeitos de estabilização, a molécula pode existir em várias formas tautoméricas que estão em equilíbrio umas com as outras. A hipoxantina é composta de cristais sólidos transparentes que derretem a 250 graus. Não se dissolve em água fria ou álcool. No entanto, é facilmente solúvel em água quente, ácidos ou álcalis.
Função, efeito e tarefas
Como mencionado, a hipoxantina é um produto intermediário na degradação das bases purinas. A enzima xantina oxidase oxida-a em xantina. Juntamente com a xantina, é então decomposto em ácido úrico com a ajuda da xantina oxidase. A diferença entre hipoxantina e xantina é que a xantina também possui um grupo hidroxila ligado à posição 2.
Além disso, a hipoxantina pode ser decomposta em ácido úrico e realimentada no metabolismo das purinas por meio da via de resgate.Em contraste, a xantina só se decompõe em ácido úrico. A hipoxantina e a ribose formam o nucleosídeo inosina. A inosina é incorporada ao anticódon do tRNA em casos muito raros. É usado na produção de primers degenerados que iniciam uma reação em cadeia da polimerase. É uma base neutra que pode emparelhar com todas as nucleobases. No entanto, o emparelhamento com a citosina é energeticamente o melhor.
Outro composto importante derivado da hipoxantina é o monofosfato de inosina. Este composto é um éster de ácido fosfórico de inosina. Monofosfato de inosina (IMP) é um intermediário chave para a síntese de monofosfato de guanosina (GMP) e monofosfato de adenosina (AMP), os quais podem ser usados novamente para a síntese de ácido nucleico. A síntese do ME ocorre a partir da hipoxantina diretamente pela via de resgate. As duas enzimas AICAR formiltransferase / IMP ciclase e hipoxantina guanina fosforibosiltransferase são amplamente responsáveis por isso. Assim, a hipoxantina fica na interface entre a quebra das bases purinas para formar ácido úrico e o acúmulo de ácidos nucléicos. Monofosfato de inosina também é usado como intensificador de sabor.
Educação, ocorrência, propriedades e valores ideais
A hipoxantina é formada como um produto intermediário no metabolismo das purinas e está no limiar entre a quebra e a reconstrução das bases das purinas. Se for oxidado em xantina pela enzima xantina oxidase, a reação reversa às nucleobases adenina e guanina não será mais possível.
A hipoxantina é produzida a partir da base de adenina purina, enquanto a quebra da guanina leva à xantina. No entanto, as reações dos vários nucleosídeos e nucleotídeos estão ligadas entre si por meio de uma rede complicada. Os nucleotídeos de adenosina levam diretamente à hipoxantina, com AMP como a substância-chave. No entanto, o GMP também pode ser convertido em AMP via IMP e adenilossuccinato. O AMP então leva à hipoxantina por meio da formação de adenosina e inosina, entre outras coisas. Além da guanina e da adenina, a hipoxantina também pode produzir nucleotídeos como blocos de construção de ácido nucleico por meio da via de resgate.
Você pode encontrar seu medicamento aqui
➔ Medicamentos para a saúde da bexiga e do trato urinárioDoenças e distúrbios
Vários distúrbios podem surgir em conexão com a hipoxantina. Quando a purina é decomposta, a hipoxantina e a xantina são produzidas igualmente. A hipoxantina é convertida em xantina pela xantina oxidase. A mesma enzima então decompõe a xantina em ácido úrico.
No entanto, quando a xantina oxidase está ausente, a xantina e a hipoxantina acumulam-se no sangue. Os níveis de ácido úrico são muito baixos. No entanto, é principalmente a concentração de xantina que aumenta, porque a hipoxantina tem a opção de ser reciclada pela via de resgate. O quadro clínico de xantinúria se desenvolve. A excreção de xantina na urina pode aumentar em 1.500 por cento. Os valores de hipoxantina não aumentam tanto. As altas concentrações de xantina podem causar danos aos rins. Se a ingestão de líquidos for insuficiente, podem se formar cálculos renais ou no trato urinário. A excreção de cristais de urina também é possível.
Em casos muito graves, pode levar à insuficiência renal fatal. No entanto, como a xantina e a hipoxantina têm um certo grau de solubilidade em água, a melhor terapia é beber muito. Alimentos ricos em purinas, como peixes, mexilhões, legumes ou cerveja, devem ser evitados. No entanto, também existem formas mais graves de xantinúria. Além de doenças renais graves, isso pode levar a atrasos no desenvolvimento intelectual, autismo ou até distúrbios de desenvolvimento dentário. Uma vez que a hipoxantina também pode ser reciclada por meio da via de recuperação, ao contrário da xantina, as interrupções dentro desse processo levam ao aumento da formação de ácido úrico, porque apenas a via de degradação da base purina funciona.
A hipoxantina resultante só pode ser oxidada em xantina, que por sua vez é convertida em ácido úrico. Freqüentemente, há um defeito hereditário na enzima hipoxantina guanina fosforibosil transferase. A concentração de ácido úrico no sangue aumenta drasticamente, o que pode levar à precipitação de cristais de ácido úrico nas articulações. O resultado são ataques de gota. Em casos graves, desenvolve-se a síndrome de Lesch-Nyham.

.jpg)




.jpg)


.jpg)







.jpg)