o potencial pós-sináptico excitatório é um potencial excitante na membrana pós-sináptica dos neurônios. Os potenciais individuais são somados espacial e temporalmente e podem, assim, criar um potencial de ação. Os distúrbios de transmissão, como miastenia gravis ou outras miastenias, interrompem esses processos.
Qual é o potencial pós-sináptico excitatório?

Os neurônios são separados uns dos outros por um gap de 20 a 30 nm, também conhecido como gap sináptico. É a lacuna mínima entre a região da membrana pré-sináptica de um neurônio e a região da membrana pós-sináptica da célula nervosa a jusante.
Os neurônios transmitem excitação. Portanto, sua lacuna sináptica é preenchida pela liberação de substâncias mensageiras bioquímicas, também conhecidas como neurotransmissores. Isso cria um potencial pós-sináptico excitatório na região da membrana da célula a jusante. É uma alteração localmente limitada no potencial de membrana pós-sináptica. Essa mudança gradual no potencial desencadeia um potencial de ação no elemento pós-sináptico. O potencial pós-sináptico excitatório faz parte da condução da excitação neuronal e surge quando a membrana celular a jusante é despolarizada.
Os potenciais pós-sinápticos excitantes são recebidos e processados pelo neurônio seguinte, somando-se tanto espacial quanto temporalmente. Quando o potencial limite da célula é excedido, um potencial de ação recém-formado é carregado pelo axônio.
O oposto do potencial pós-sináptico excitatório é o potencial pós-sináptico inibitório. Isso leva à hiperpolarização da membrana pós-sináptica, o que impede o desencadeamento de um potencial de ação.
Função e tarefa
O potencial pós-sináptico excitante e o potencial pós-sináptico de inibição afetam todas as células nervosas. Quando seu potencial de limiar é excedido, as células nervosas despolarizam. Eles respondem a essa despolarização liberando neurotransmissores excitatórios. Uma certa quantidade dessas substâncias ativa os canais iônicos sensíveis ao transmissor no neurônio. Esses canais são permeáveis aos íons potássio e sódio. Potenciais locais e graduados no sentido de um potencial excitatório despolarizam a membrana pós-sináptica do neurônio.
Quando o potencial de membrana é derivado intracelularmente, o potencial pós-sináptico excitatório é a despolarização da membrana soma. Esta despolarização ocorre como resultado da propagação passiva. Existe um somatório de potenciais individuais. A quantidade de neurotransmissor liberado e o tamanho do potencial de membrana prevalecente determinam a extensão do potencial pós-sináptico excitatório. Quanto maior a pré-despolarização da membrana, menor o potencial pós-sináptico excitatório.
Se a membrana já estiver despolarizada acima de seu potencial de repouso, o potencial excitatório pós-sináptico cai e, em certas circunstâncias, chega a zero. Nesse caso, o potencial de reversão do potencial excitatório é alcançado. Se a pré-despolarização for ainda maior, surge um potencial com sinal oposto. Assim, o potencial pós-sináptico excitatório nem sempre deve ser equiparado a uma despolarização. Ele move a membrana em direção a um certo potencial de equilíbrio, que freqüentemente permanece abaixo do respectivo potencial de membrana em repouso.
O trabalho de um mecanismo de íon complexo desempenha um papel nisso. Com o potencial pós-sináptico excitatório, pode-se observar um aumento da permeabilidade da membrana para os íons potássio e sódio. Por outro lado, também podem ocorrer potenciais com condutividade reduzida para íons sódio e potássio. Nesse contexto, acredita-se que o mecanismo do canal iônico seja o gatilho para o fechamento de todos os canais iônicos de potássio com vazamento.
O potencial pós-sináptico inibitório é o oposto do potencial pós-sináptico excitatório. Também aqui o potencial de membrana muda localmente na membrana pós-sináptica das células nervosas. A hiperpolarização da membrana celular ocorre na sinapse, o que inibe o desencadeamento de potenciais de ação dentro da estrutura do potencial pós-sináptico excitatório. Os neurotransmissores nas sinapses inibitórias desencadeiam uma resposta celular. Os canais da membrana pós-sináptica se abrem e permitem a passagem de íons de potássio ou cloreto. A saída do íon potássio resultante e o influxo do íon cloreto causam a hiperpolarização local na membrana pós-sináptica.
Você pode encontrar seu medicamento aqui
➔ Remédios para fraqueza muscularDoenças e enfermidades
Várias doenças interrompem a comunicação entre as sinapses individuais e, portanto, também a transdução de sinal na sinapse química. Um exemplo é a doença neuromuscular miastenia gravis, que afeta a placa terminal muscular. É uma doença autoimune de causa previamente desconhecida. No caso da doença, o corpo forma autoanticorpos contra os tecidos do próprio corpo. Na doença muscular, esses anticorpos são direcionados contra a membrana pós-sináptica das placas terminais neuromusculares. Na maioria das vezes, os autoanticorpos nessa doença são anticorpos do receptor de acetilcolina. Eles atacam os receptores nicotínicos da acetilcolina nos pontos de conexão entre os nervos e os músculos. A inflamação imunológica resultante destrói o tecido local.
Como resultado, a comunicação entre o nervo e o músculo é perturbada, uma vez que a interação entre a acetilcolina e seu receptor é dificultada ou mesmo impedida pelos anticorpos do receptor da acetilcolina. O potencial de ação não pode mais passar do nervo para o músculo. O músculo, portanto, não é mais excitável.
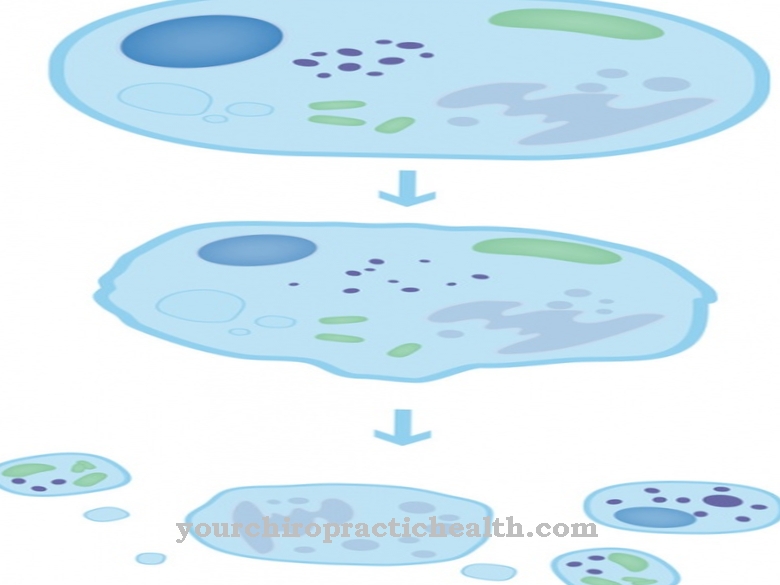
A soma de todos os receptores de acetilcolina é reduzida ao mesmo tempo que os receptores são destruídos pela atividade imunológica. As membranas subsinápticas se desintegram e a endocitose cria um autofagossomo. As vesículas de transporte se fundem com os autofagossomos e os receptores de acetilcolina mudam como resultado dessa reação imunológica. Com essas mudanças, toda a placa terminal do motor muda. A lacuna sináptica se alarga. Por esse motivo, a acetilcolina se difunde para fora da fenda sináptica ou é hidrolisada sem se ligar ao receptor.
Outras miastenias mostram efeitos semelhantes na fenda sináptica e no potencial pós-sináptico excitatório.






.jpg)



.jpg)
.jpg)